딥러닝 모델을 이용한 대장내시경 검사 중 대장 선종병변과 증식성용종의 실시간 감별 연구
Real-time differentiation of adenomatous and hyperplastic diminutive colorectal
polyps during analysis of unaltered videos of standard colonoscopy using a deep learning model
(Gut 2019;68:94–100)
아주 작은 용종의 제거 후 병리 검사를 시행하지 않고 폐기하는 “resect and discard” 를 하기 위해서는 작은 선종성 병변과 증식성용종 병변을 내시경 소견으로 잘 구분할 수 있어야 합니다. 하지만 내시경 초심자 뿐만 아니라 경험이 많은 내시경 전문의도 두가지 병변을 정확하게 감별하기는 어려움이 있습니다. 아주 작은 용종의 “resect and discard” 를 시행하기 위하여 인공지능 딥러닝 모델을 활용하여 대장내시경 검사 중 실시간으로 용종에 대한 정보를 전달하는 연구가 최근 보고되었습니다. 125개의 대장내시경 비디오에서 선종과 증식성용종을 구분할 수 있는지를 보았고, 정확도는 94% (95% CI 86% to 97%), 선종을 감별하는 민감도는 98% (95% CI 92% to 100%), 특이도는 83% (95% CI 67% to 93%), 음성예측도 97%, 양성예측도는 90% 이었습니다. 실제 환자의 대장내시경검사에서도 이 딥러닝 모델을 이용하여 “resect and discard” 를 시행하는 것이 타당한지를 보는 연구가 앞으로 필요합니다.
- 주요 내용 요약 -
- 아주 작은 미세 대장 용종을 제거하여 병리 검사를 시행하는 번거로움과 비용증가를 줄이기 위하여 “resect and discard” 개념이 제시되었지만 초심자 및 경험이 많지 않은 내시경 전문의에게는 이와 같은 실시간 선종/증식성용종 감별 딥러닝 알고리즘이 도움이 될 수 있습니다.
- 별도의 이미지 변환 과정 없이 일반적인 내시경 영상으로 트레이닝된 인공지능 알고리즘으로 정확도가 94%로 높은 결과를 보였고 약 50ms 의 시간지연으로 거의 실시간 정보 제공이 가능하였습니다.
- 의료비용 증감과 업무과중을 줄이기 위한 대장미세용종의 “resect and discard”는 더 일상적인 대장내시경 검사 및 시술에 정착되기 위해서 이와 같은 인공지능 플랫폼이 많은 도움이 될 것입니다.
논문 바로가기 ▶
췌관내 유두상 점액종양의 치료
한림대학교성심병원 소화기내과 문성훈
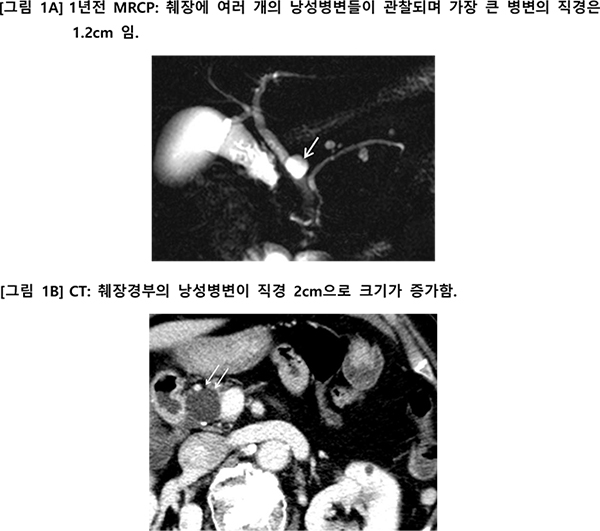
69 세 여자 환자가 4년전부터 추적관찰 해오던 췌장의 낭성병변 낭성병변 에 대한 검사를 위하여 내원하였 습니 다. 기저질환으로는 당뇨병 과 골다공증 이 있어서 복약 중이었지 만 그 외 전신상태는 건강하였 습니 다. 췌장의 낭성병변 은 췌장 경부부터 미부까지 여러 개가 있었 으며 가장 크기가 컸던 병변은 췌장 경부에 있으며 1년전 MRCPMRCPMRCPMRCP에서 1.2 cm 이었고 최근 CT 에서 2.0cm .0cm으로 크기가 증가하였고 사진은 다음과 같습니다 .
+본문 전체보기
- 질문
- 환자에게 다음에 다음에 시행할 검사는 무엇입니까 ? 환자의 낭성종양의 크기의 증가가 2년동안 5mm 이상이어서 초음파내시경 검사를 검사를 시행하였습니다 .
- 해설
- 2012년 Fukuoka 가이드라인이 발표되었고 이후 2017년에는 Fukuoka 가이드라인을 일부 수정하여 개정된 국제 가이드라인(Revision of international consensus Fukuoka guidelines for the management of IPMN of the pancreas)을 발표하였습니다. Fukuoka 가이드라인에서는 "worrisome feature"가 있으면 초음파내시경 시행을 권고하고 있는데 2017년 개정된 worrisome feature는 다음과 같이 확장되었습니다.

- 질문
- 환자의 초음파내시경에서 5.8mm크기의 벽결절(mural nodule)이 관찰되었으며, 체위의 변화에 따라서 움직이지 않았습니다(그림 2). 환자에게 초음파내시경 유도 아래 세침흡인을 시행하여 4cc 정도의 약간 끈적끈적한 무색의 액체를 획득하 였습니다. 흡인된 낭액에서 시행해야 할 검사는 무엇일까요?
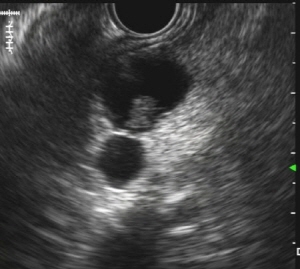
흡인된 낭액에 대하여 세포진검사, CEA, 아밀라아제 검사를 시행하였습니다. 낭액의 CEA는 880 ng/mL이었으며 아밀라아제는 1020 U/L이었으며 세포진 검사에서 악성세포는 관찰되지 않았습니다.
- 해설
- 2017년 개정된 국제 가이드라인에 따르면 초음파내시경 유도하 낭액 검사는 낭액의 누출(leakage)에 대한 우려로 인하여 적극 추천되지는 않지만 다음과 같은 해석을 첨부하고 있습니다. CEA >192-200 ng/mL의 기준치는 점액성 낭(췌관내 유두상 점액종양 또는 점액성 낭성종양)의 진단에 있어서 80% 정도의 정확도를 가집니다. 아밀라아제는 췌관내 유두상 점액종양에서 모두 높지는 않고 점액성 낭성 종양에서도 높은 경우가 있습니다. 세포진 검사의 민감도는 낮지만 이형성세포나 악성세포가 관찰될 수 있습니다.
- 질문
- 본 환자에서 어떤 수술을 시행하는 것이 좋을까요?
담당의사는 본 환자가 수술에 적합한 전신상태이며 벽결절이 관찰되어서 췌십이 지장 절제술을 시행하였습니다. 췌장 체부와 미부의 병변들은 1cm미만이어서 경과 관찰하기로 하였습니다.
- 해설
- 2017년 개정 국제 가이드라인에서 췌장 절제술의 적응증은 다음과 같습니다.
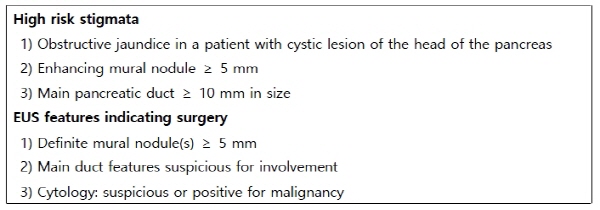
- 질문
- 환자에서 췌장 절제검체에 대한 병리검사에서는 고도이형성의 췌관내 유두 상 점액종양으로 진단되었고 절제면은 종양의 침범이 없었습니다. 남아 있는 췌장에 는 1cm미만 크기의 낭성병변이 남아 있었습니다. 환자에서 추적을 위한 다음 영상 검사는 언제 시행하는 것이 추천될까요?
본 환자의 절제면에 종양의 침범이 없고 남아 있는 낭성병변은 1cm미만 크기이며 최근 4년간 변화가 없었던 병변이어서 2-3년 뒤에 CT나 MRI로 추적검사 할 계획입 니다.
- 해설
- 22017년 개정된 국제 가이드라인에 따르면 절제면이 정상이거나 PanIN-1A or -1B 이면 음성절제면으로 분류하고, 남아 있는 췌장의 잔여 병변은 절제하지 않은 췌관내 유두상 점액종양의 추적방법에 따릅니다.
1기 식도편평세포암에서 내시경 절제술과 선택적 항암화학방사선요법의 효용성
Efficacy of Endoscopic Resection and Selective Chemoradiotherapy for Stage I Esophageal Squamous Cell Carcinoma
(Gastroenterology 2019;157:382-390)
식도암의 내시경 절제술의 적응증은 위암보다 협소하고 연구도 상대적으로 부족합니다. 식도암 1기의 표준치료는 수술적 절제술이지만, 항암화학요법도 수술 사망률, 이환률 및 장기 보존의 관점에서 관심을 모으고 있습니다. 본 연구는 비록 비교연구는 아니지만, 내시경 절제술 후 점막암(T1a)으로 완전 절제되어 경과 관찰한 군(A), 점막하암(T1b) 이거나 점막암이지만 림프혈관침범이 있어 항암화학방사선요법을 시행한 군(B), 불완전절제되어 항암화학방사선요법을 시행한 군(C)을 전향적으로 3년간 비교하였습니다.
- 주요 내용 요약 -
- 전체 환자의 3년간 overall survival(OS)은 92.6% 였고, B군은 90.7% 였습니다.
- 3년간 재발은 전체적으로 8.5% 였다. A, B, C군 각각 1.4%, 11.5%, 26.7% 였습니다.
- 본 연구는 수술과 직접 비교가 아니라는 제한점이 있으며, 연구 기간과 참여 기관수에 비해 연구 규모가 작은 아쉬움이 있습니다.
- 그럼에도 불구하고 장기 보전을 목표로 하는 새로운 다학제치료 (내시경 절제술 + 항암화학방사선요법)의 효용성을 보여주어 후속연구가 기대됩니다.
논문 바로가기 ▶





